
隨著人工智慧(AI)與機器人技術的深度整合,人類與機器的互動方式正迎來革命性發展。根據研調機構 IMARC Group 最新市場報告顯示,日本腦機介面(Brain-Computer Interface, BCI)市場展現出強勁的成長動能。2025 年日本 BCI 市場規模已達 1.602 億美元,預計到 2034 年將大幅擴張至 6.252 億美元,2026 年至 2034 年間的年均複合成長率有望(CAGR)高達 16.34%。
BCI 市場得以高速成長,AI 技術的介入是關鍵轉捩點;過去,腦電波訊號極易受到噪訊干擾,導致指令執行不準確,但現在 AI 演算法已能有效剔除腦電圖(EEG)中的偽影與干擾,從數十億個神經元產生的複雜電活動中識別出有意義的神經模式。
日本作為全球高齡化程度最深的國家之一,對於神經系統疾病(如中風、肌萎縮性脊髓側索硬化症 ALS、脊髓損傷)的醫療輔助需求迫切。日本政府積極推動輔助技術開發與無障礙政策,為 BCI 商業化營造有利的監管環境。
此外,非侵入式 BCI 技術的進步,排除掉傳統侵入式系統需手術的高風險與限制,大幅降低了用戶的採用門檻,使得該技術從醫療臨床擴展至家庭護理與消費者市場。
根據最新產業動態,日本各大機構與企業已展開頻繁布局:
| 時間 | 機構 / 企業 | 重大技術與產品發布 |
| 2025年1月 | ATR 國際電氣通信基礎技術研究所 | 發表非侵入式 BCI 進展,實現研究參與者間直接的「腦對腦通訊」。 |
| 2024年12月 | 索尼(Sony) | 推出消費級 BCI 頭戴式裝置,具備高度訊號處理與機器學習,鎖定遊戲與娛樂應用。 |
| 2024年11月 | 理化學研究所(RIKEN) | 展示無線 BCI 控制機器人輪椅,協助重度運動障礙者實現獨立導航。 |
| 2024年10月 | NTT | 與大學合作開發 BCI 神經復健系統整合 VR 技術加速中風患者的功能恢復。 |
報告指出,日本 BCI 市場未來將呈現多元化發展。除了傳統的醫療復健、神經補綴與殘障恢復應用外,智慧家居控制、沈浸式娛樂與遊戲、以及虛擬實境(VR)中的人機交互,都將成為市場增長點。
展望 2026 年至 2034 年,隨著電子元件微型化與 AI 解碼能力持續進步,日本有望在全球神經技術產業中扮演核心角色,將前沿研究轉化為提升人類能力與生活品質的實用產品。



記者李婉如/綜合報導 2025杏輝宜蘭馬拉松記者會於114年6月2日上午10點30分,在臺北市「典空間」隆重舉行,由宜蘭縣代理縣長林茂盛與杏輝藥品總經理白友烺共同主持。現場正式宣布本屆賽事將於11月8日(星期六)在宜蘭運動公園盛大登場,邀請全國跑者齊聚宜蘭,在山海湖之間奔馳,用腳步記錄生命、用行動感受熱情。 林茂盛代理縣長表示,杏輝宜蘭馬拉松自2022年創辦以來,已成為推動運動觀光、健康城市及公益關懷的活動。今年賽事亮點包括:在地菁英跑者陳立羣再次挑戰山海賽道、71歲抗癌鬥士王啟中女士首度挑戰全馬,展現生命的韌性與希望,以及全台唯一連續三年舉辦、向醫事人員致敬的行動,傳遞對醫護人員長期守護社會的感謝與敬意。縣府將持續與杏輝藥品合作,共同將這項在地品牌賽事打造成為串聯運動、公益與觀光的重要平台,讓更多人透過馬拉松看見宜蘭的自然美景與人文溫度。 杏輝藥品總經理白友烺表示,將企業責任實踐在每一場與生命有關的行動中。透過這場馬拉松,不僅能推廣運動風氣,也是一種與民眾對話的方式,讓大家看見跑者的熱情、在地的溫度與人與人之間的連結。他強調,未來將持續與縣府攜手,深化品牌與地方的合作關係,讓宜蘭的美好被更多人「用腳步走進心裡」。 今年賽事補給全面升級,沿途提供小農點心與國宴等級的宜蘭美食,讓跑者在挑戰自我之餘也能大飽口福。為鼓勵不同階段的跑者持續前進,大會推出「馬拉松尊榮禮遇」方案,首度挑戰半馬、全馬或完成第50馬、第100馬者,皆可獲得專屬紀念獎盃與500元交通補助(限額共50名)。同時延續「為您而笑」醫事人員感謝行動,設立專屬獎項並邀請醫事跑者參與現場微笑儀式,向守護健康的第一線英雄致敬;更同步發起「#為您而笑」社群串連活動,邀請民眾上傳微笑照片與感謝語,一起傳遞正能量。 即日起,2025杏輝宜蘭馬拉松正式開放報名,報名截止日期為8月8日。宜蘭縣政府誠摯邀請全國跑者與民眾,一起踏上這條融合山海湖風景、生命故事與公益精神的賽道。不論你是初馬挑戰者、經驗老將,或是為夢想奔跑的你,都能在宜蘭找到專屬自己的節奏與感動。讓我們11月8日相約宜蘭,一起用雙腳跑出屬於自己的勁情紀錄! 此篇文章最開始出處為: 2025杏輝宜蘭馬拉松記者會登場



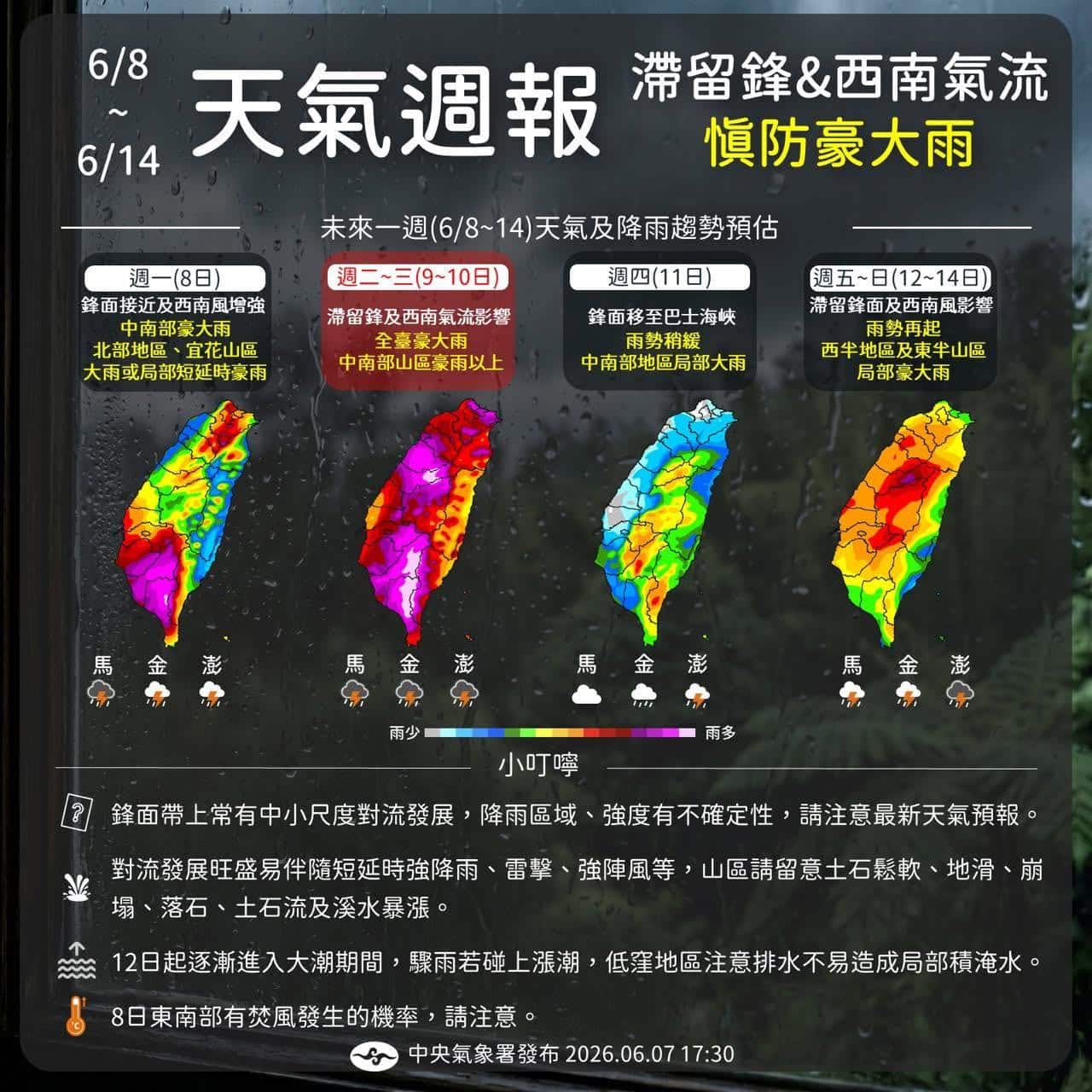
根據氣象署預報,6月8日至14日滯留鋒面及西南氣流報到,慎防劇烈降雨及強風大浪。嘉義縣政府籲請養殖漁業要做好防汛準備,注意水質與底土管理,必要時提早收成,避免損失。 縣府農業處提醒魚塭養殖業者,應加強塭堤修補維護和排水設施疏通,檢視發電機能否正常使用並添足用油,加強巡視水閘門保持操作正常,必要時請於塭堤加設防護網,以減少魚塭溢堤或潰堤時,因養殖物流失造成損失,雷雨期間也要預防雷擊。 尤其梅雨滯留鋒影響及西南氣流影響期間,會伴隨強陣風及大浪,請淺海牡蠣養殖業者,必須檢查設施結構,妥為裝修補強,必要時應提早收成,避免造成蚵棚危害損失。 梅雨鋒面常帶來大量雨水,造成養殖魚塭生態改變,包括水溫、鹽度、pH降低,濁度增加,以及浮游生物死亡,同時這段期間也伴隨低氣壓吹南風,天氣型態悶熱多雨,魚塭之水中溶氧降低,水體中甲烷及硫化氫含量會增加,易引起池中養殖生物緊迫、食慾減退,甚至疾病死亡。 養殖戶應多加關注天氣變化,加強觀察魚塭狀況,必要時減少投餵數量、投餵頻率,增加水車啟動頻率,適時調整水位,可排放上表層雨水,減緩水質惡化的發生情形。大雨來臨或過後,可以適時添加益生菌或水質改善劑,增加緩衝能力以穩定水質,避免水產生物疾病問題。 若養殖戶有水質檢驗需求,或遇水產物異常或疾病情形,可將池水或魚隻檢體送至家畜疾病防治所(太保市太保一路1號、05-3620025)、東石水產動物疾病檢驗中心(東石鄉副瀨村新結庄14-2號、05-3734330)或水產動物疾病防治中心(義竹鄉新店村2-6號、05-3427922),由獸醫師提供檢診及諮詢服務。 如發生漁業災損,請及時向公所及漁會通報,並多運用「農產業天然災害現地照相」APP,記錄受災情形,保障自身權益及提高救災效率。 圖/嘉義縣政府提供




記者李婉如/綜合報導 你手中的工具,只是生冷的鋼鐵,還是最懂你的夥伴?全球頂尖工具品牌博世(Bosch)今天在台灣帶來了令人振奮的消息——全新「專業手工具」與「專業 VDE 絕緣手工具」系列正式登陸台灣!這一次,博世不僅為水電工程師、電機師傅帶來了跨時代的安全防護,更用「20年保固」的超狂承諾,寫下對台灣職人們最深情的告白。 是頂級職人的靈魂,也是 3C、模型玩家的夢幻逸品 博世深知,無論是頂著烈日在工地施工的裝修師傅,還是在工作室裡挑燈夜戰、改裝電腦硬體與組裝精密模型的科技玩家,對於工具的「手感」都有著近乎挑剔的執著。 全新博世專業手工具系列(鉗類、起子、扳手、測量工具等),特別導入了防滑握柄與平衡施力設計。拿在手上的那一刻,就能感受到完美的人體工學,即便是長時間高強度的使用,也能大幅減輕手部疲勞,讓你的每一次發力都精準到位、流暢無比。 用最高規格,守護每一位無名英雄的安全 針對需要接觸高壓電力的配電、新能源與智慧家居維修職人,博世特別推出了「專業 VDE 絕緣手工具」。 雙色外衣,安全一眼看穿: 亮眼的雙色包覆設計,讓你在高風險的活電現場,一眼就能確認工具是否完好安全。 萬伏特測試的極致守護: 每把工具都通過 10,000V 的嚴格考驗,擁有符合國際標準的 1,000V 安全防護。面對高溫、高衝擊的嚴苛環境,它就是你最強大的安全後盾。 承諾,從現在開始延續 台灣博世電動工具業務部總經理賀文廣感性表示,工具是職人每天並肩作戰的夥伴。正因為明白這層羈絆,博世承諾這系列手工具將陪伴你走過未來的 20 年。且從今年(2026年)開始,博世將陸續推出高達數百款新品,滿足你對各種修繕與創作的渴望。 【新品上市好康報報】 博世專業手工具與 VDE 絕緣手工具即日起已在全台授權經銷商正式上架!現在購買還能享有「新品滿額贈」與「開箱贈獎」等多重好禮。想升級你的工具箱嗎?快到博世官網或臉書粉絲專頁一探究竟! 博世專業手工具與 VDE 絕緣手工具即日起於全台授權經銷商開始販售,並同步推出新品滿額贈與開箱贈獎等多重回饋活動。詳細內容可至博世電動工具官方網站以及臉書粉絲專頁查詢。 更多專業手工具產品相關訊息請聯絡: 台灣博世電動工具業務部柯昌廷先生(洽詢電話:+886-2-7734-9504)


