是新聞網 記者/林偉志

圖/unsplash
為掌握未來躍升台股前50大企業的新星股票,復華投信最新推出「復華台灣未來50主動式ETF基金(基金之配息來源可能為收益平準金)」,募集期間為2025/12/3至12/5,只要新臺幣1萬元,即可在復華投信或各大券商,搶先卡位未來50的潛力!
這檔主動式ETF的特色?
「00991A主動復華未來50(基金之配息來源可能為收益平準金)」是從市值前150大的台灣上市、上櫃公司中**,以主動研究方式,挑出未來可能成為市值前50大的公司,追求長期打敗台灣加權指數,可提供投資人無論是長線布局或波段操作,均有機會提供投資人掌握台灣未來主要的經濟成長動力。
四大選股方法,發掘價值成長股及轉機股
復華投信觀察到台灣50指數成分股的變化,於是推出全新主動式ETF,透過以下四大選股方法,進一步發掘價值成長股及轉機股:
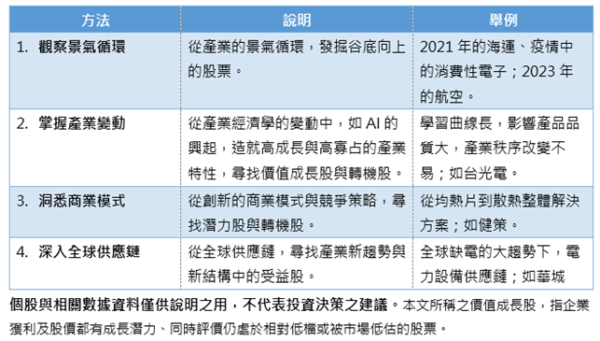
投資台股一魚兩吃:長線布局、波段操作皆宜
「00991A主動復華未來50(基金之配息來源可能為收益平準金)」不僅是一檔長期投資工具,也具備波段操作的特性。對於想透過長期複利效果累積財富的投資人,本基金以基本面研究與產業趨勢選股為基礎;而對於擅長波段操作的投資人,基金因波動度較高,也能提供短線進出的靈活空間。
值得留意的是,復華投信的研究團隊,涵蓋全球總體經濟、股市及債市,有能力從全球產業分工發掘產業趨勢,歷年來更囊括多項投資研究團隊大獎,例如2021年榮獲理柏台灣基金獎 – 整體團隊大獎,為該獎項成立以來,首度由本土投信獲獎。此外,復華投信多年來共獲得10座Smart智富台灣基金獎的團隊獎項,數量更是傲視投信同業。

12/3~12/5募集,1萬元買起來
「00991A主動復華未來50(基金之配息來源可能為收益平準金)」將在2025/12/3至12/5進行募集,每單位發行價格為新臺幣10元,即每張最低只要新臺幣1萬元,即可在復華投信或各大券商,搶先卡位未來50的潛力!
*本文所稱之台灣50,指台灣股市中市值前50大的公司。
**本基金預計以市值前150大之上市上櫃股票為主要選股池;基金資產配置將視當時投資環境調整;基金投資方針與特色詳見公開說明書。
***本文所稱之台灣加權指數,指臺灣證券交易所發行量加權股價報酬指數。

※免責聲明:文中所提之個股內容,並非任何投資建議與參考,請審慎判斷評估風險,自負盈虧。


圖/本報AI製圖(示意圖) 商傳媒|葉安庭/綜合外電報導 製藥大廠因應現任美國總統川普(Donald Trump)政府推行的藥品定價政策轉變,正策略性地延遲新藥在歐洲上市,此舉旨在維持美國市場的較高藥價,避免受歐洲低價影響。此項定價策略已對全球藥品定價模式造成複雜影響,並衝擊歐洲病患取得新療法的機會。 川普政府正積極推動將美國處方藥價格與歐洲等其他富有國家較低的藥價掛鉤,此政策被稱為「最惠國待遇」定價,或「國際參考定價制度」。由於美國藥價傳統上遠高於其他國家,藥廠擔憂若在新藥於歐洲市場推出時接受較低價格,恐將反過來影響其在美國市場的定價權,進而損害營收。 自國際參考定價制度於去年五月實施以來,歐洲新藥上市的數量已大幅下降約 35%。這項策略性暫停不僅打亂了藥廠的全球藥品分銷計畫,也使他們與歐洲醫療政策制定者的關係變得複雜。儘管此舉有助於藥廠維持美國市場的高收益,但同時也讓歐洲病患無法及時獲得所需的創新治療。




(示意圖:Gemini生成) 她每天都很忙。 行程滿滿、訊息很多、 事情一件接一件。 但有一天,她突然發現—— 自己其實說不出來, 這些忙,到底是為了什麼。 不是沒有目標, 而是太多「應該要做的事」。 應該回訊息、 應該把事情做好、 應該不要讓別人失望。 久了之後,生活變成一種「反射動作」。 她開始嘗試停下來, 把每天的時間留一點空白。 沒有安排、沒有目的, 只是發呆、散步、或坐著。 一開始很不習慣,甚至有點焦慮。 但慢慢地,她發現—— 原來自己不是需要更多時間, 而是需要一點「屬於自己的時間」。 很多人看起來很努力, 但其實只是沒有停下來的機會。 有時候,慢一點, 不是退步,是重新找回方向。



圖/本報AI製圖(示意圖) 商傳媒|康語柔/綜合外電報導 全球製藥產業近期迎來多項重要進展,涵蓋癌症治療、心血管疾病及新陳代謝領域,同時監管機構也對藥廠的法規遵循提出警示。 輝瑞攝護腺癌療法顯著改善患者預後 製藥巨頭輝瑞(Pfizer)旗下PARP抑制劑「Talzenna」(talazoparib)與「Xtandi」(enzalutamide)的合併療法,在治療帶有同源重組修復(HRR)基因突變的轉移性賀爾蒙敏感性攝護腺癌(mHSPC)上取得顯著突破。根據TALAPRO-3第三期臨床試驗結果,該組合療法已達成主要評估指標,顯著延長了患者的影像學無惡化存活期(rPFS),其表現超越預設的0.63風險比(hazard ratio)。此外,初期分析也顯示出患者整體存活期(OS)改善的強烈趨勢。輝瑞預計將把這些研究數據提交至全球各地的監管機構,以尋求藥物核准。 Apixaban出血風險低於Rivaroxaban 在心血管疾病治療方面,一項於2026年3月19日發表於《新英格蘭醫學期刊》(New England Journal of Medicine)的第四期COBRRA試驗,比較了兩種常用口服抗凝血劑apixaban與rivaroxaban,在急性靜脈栓塞(VTE)患者中的表現。研究顯示,在2,760名急性VTE患者中,接受apixaban治療組的臨床相關出血率為3.3%,顯著低於rivaroxaban組的7.1%,這表示apixaban相對降低了54%的出血風險。然而,兩組患者的復發性VTE發生率則幾乎相同。研究作者認為,rivaroxaban初期每日兩次15毫克的密集給藥策略,可能是導致其出血風險較高的原因。 禮來Retatrutide展現優異減重與控糖效果 禮來(Eli Lilly)於2026年3月19日宣布,其正在研發中的三重促效劑retatrutide,在治療第二型糖尿病的TRANSCEND-T2D-1第三期臨床試驗中,成功達成所有主要與次要評估指標。這款實驗性藥物作用於GIP、GLP-1和胰高血糖素等多個受體。在為期40週的試驗期間,使用retatrutide的患者平均體重減輕達16.8%,糖化血色素(A1C)降低2.0%。特別是接受12毫克劑量的患者,平均體重減輕了36.6磅,且體重下降趨勢在治療結束時仍未見高原期,顯示其長效且顯著的減重潛力。 FDA示警諾和諾德未符安全通報要求 另一方面,美國食品藥物管理局(FDA)向諾和諾德(Novo Nordisk)發出警告信,指控其未能遵守上市後不良藥物事件的強制性通報要求。FDA的調查發現,該公司多起嚴重不良事件並未在法定期限內完成通報。FDA強調,安全通報的延遲會嚴重影響其快速有效評估真實世界藥物風險的能力,並指出及時的安全通報對於持續性藥物警戒(pharmacovigilance)至關重要,提醒臨床醫師即使面對廣泛使用且成功的藥物,仍須密切關注新的安全疑慮。


